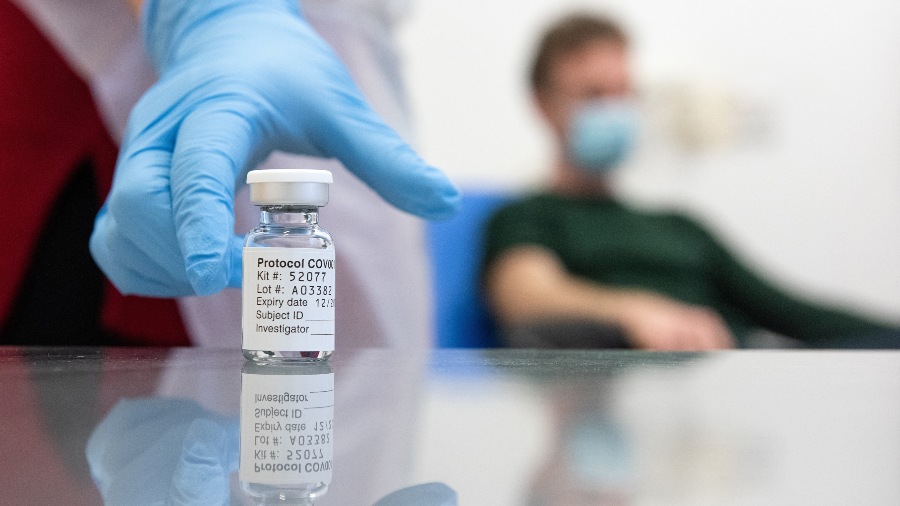
La Universidad de Oxford admiti¾ que, por equivocaci¾n, hubo “diferencias” en la forma de administrar las dosis de su vacuna contra la COVID-19 a los voluntarios en los ensayos, pero aclar¾ que los mķtodos para medir la concentraci¾n del antĒdoto han quedado ya “establecidos”.
En un comunicado este jueves, la universidad britßnica pretende despejar las crecientes dudas surgidas en los ·ltimos dĒas sobre la efectividad de hasta un 90 % que se observ¾ en el subgrupo que recibi¾ primero media dosis y despuķs una dosis completa del producto que ha desarrollado con la farmacķutica sueco-britßnica AstraZeneca.
Nayib Bukele, presidente de El Salvador, confirm¾ el miķrcoles que hay un acuerdo con AstraZeneca y su Gobierno por 2.5 millones de dosis de esta vacuna, pero una vez que la misma pase por los controles internacionales necesarios.
VEA TAMBIÉN: Vacuna de AstraZeneca contra el COVID-19 serß gratuita en El Salvador, dice Gobierno
Tras haber anunciado el pasado dĒa 23 los resultados preliminares de la tercera fase de las pruebas, la universidad reconoce de manera implĒcita que a la hora de suministrar las dosis a los participantes de los ensayos se parti¾ de un error.
Pascal Soriot, CEO de Astra Zeneca, dijo este jueves que la compa±Ēa harß otro “estudio internacional” de alcance global para validar la eficacia de la vacuna, y descartar las dudas sobre la protecci¾n que brinda la misma contra el COVID-19.
“Ahora que hemos encontrado lo que parece ser una mejor eficacia, tenemos que validarlo, asĒ que necesitamos hacer un estudio adicional”, expres¾ Soriot, quien agreg¾ que es un estudio “que deberĒa ser mßs rßpido, porque sabemos que la eficacia es alta y por eso necesitamos un n·mero mßs bajo de pacientes”.
Agreg¾ que esperan que este nuevo estudio no frene la producci¾n masiva de la vacuna, ni afecte el aval de las autoridades reguladoras a nivel mundial, para su posterior distribuci¾n en los distintos paĒses, de ser posible a partir de diciembre.

El grupo de expertos de la empresa, liderado por Andrew Pollard y Sarah Gilbert, inform¾ en un principio el lunes que la vacuna, ofrecida en dos dosis – preparatoria y de refuerzo-, es efectiva en una media del 70,4 %, aunque la variaci¾n en la cantidad de cada dosis afecta al resultado.
Cuando se administra media dosis seguida de una dosis completa, el nivel de eficacia asciende al 90 % -y reduce la transmisi¾n- y desciende al 62 % cuando los voluntarios reciben dos dosis enteras del antĒdoto.
Tras el anuncio, se supo que las diferencias en la cantidad de las dosis administradas entre los diferentes grupos parten de una equivocaci¾n y que la dosis que obtuvo una eficacia del 90 % se adjudic¾ a un grupo con muchos menos participantes, lo que para algunos implica cuestionar los resultados.
En su nota, la universidad explica que en su estudio “se emplearon dos niveles de dosis, basados en la misma medida de la concentraci¾n empleada en la fase I pero, como resultado de una diferencia en el proceso de manufactura para el ·ltimo estudio, se demostr¾ posteriormente que este mķtodo sobreestim¾ la dosis en los nuevos lotes, lo que result¾ en la administraci¾n de media dosis como primera dosis”.
El fallo en esa manufactura fue de una empresa contratada por AstraZeneca, seg·n detall¾ la compa±Ēa britßnica. Menelas Pangalos, ejecutivo de AstraZeneca, dijo a la agencia Reuters el lunes que la compa±Ēa no aplic¾ intencionalmente la mitad de la dosis a ning·n participante, pero calific¾ este error como “serendipia”, es decir, un descubrimiento positivo descubierto por fortuna.
Agreg¾ la empresa que “cuando qued¾ patente que se habĒa usado una dosis menor” se traslad¾ la cuesti¾n al regulador y se acord¾ un plan para probar esa combinaci¾n, permitiendo al equipo investigador “incluir ambos planteamientos en la fase III del ensayo”.
Foto AFP
“Los mķtodos para medir la concentraci¾n han quedado ya establecidos y podemos asegurar que todos los lotes de la vacuna son ahora equivalentes”, concluye la nota.
Por su parte, un portavoz de AstraZeneca defendi¾ que el ensayo se realiz¾ “ateniķndose a los mayores estßndares” y anticip¾ que se llevarßn a cabo mßs anßlisis para establecer la duraci¾n de la protecci¾n que ofrece la vacuna. Seg·n el presidente de El Salvador, Nayib Bukele, les han informado que harßn 60,000 pruebas mßs.
Seg·n el diario “Financial Times”, el responsable del programa de financiaci¾n para el desarrollo de vacunas de EE.UU., Moncef Slaoui, revel¾ el pasado dĒa 24 que el subgrupo -de apenas 2.300 personas- que recibi¾ la dosis mßs efectiva se limit¾ a individuos menores de 55 a±os, con menor riesgo de desarrollar sĒntomas severos de COVID, un dato que no divulgaron ni la universidad ni AstraZeneca al presentar sus datos.
Por ello, Slaoui baraja la posibilidad de que la diferencia en la eficacia de la vacuna haya sido “fortuita”.
CientĒficos y expertos de la industria dijeron que este error en el procedimiento de las pruebas ha minado la confianza en los resultados de la vacuna.
Seg·n un artĒculo del New York Times, AstraZeneca cometi¾ otra acci¾n irregular al reunir los resultados de dos ensayos clĒnicos realizados con operaci¾n distinta en Inglaterra y Brasil, una acci¾n que rompe las reglas en este tipo de ensayos para validaci¾n de nuevos medicamentos.
Natalie Dean, bioestadĒstica y experta en dise±o de vacunas en la Universidad de Florida, critic¾ en redes sociales esta unificaci¾n de estudios hechos en distintos lugares. “Simplemente no puedo entender de d¾nde viene toda la informaci¾n y c¾mo se combina”, dijo, y consider¾ que con estas prßcticas AstraZeneca y Oxford “obtienen una mala calificaci¾n de transparencia y rigor cuando se trata de los resultados de los ensayos de vacunas se han reportado”.
Stephanie Caccomo, portavoz de la Adminitraci¾n de Alimentos y Medicamentos de EE. UU. (FDA), se neg¾ a comentar para el New York Times sobre si este error en la dosificaci¾n de Astrzeneca podrĒa provocar que la vacuna no sea aprobada. En todo caso, la FDA expres¾ antes que apoyarß las vacunas que alcancen al menos un 50% de efectividad para prevenir o disminuir el impacto del COVID-19 en las personas, un lĒmite que la medicaci¾n de AstraZeneca ya ha superado, incluso entre los candidatos que recibieron las dos dosis completas.