Un rayo de esperanza surgió el miércoles en la lucha contra el nuevo coronavirus al anunciarse resultados prometedores de un nuevo medicamento antiviral, mientras la pandemia hundió a Estados Unidos, la primera economía mundial, en la peor recesión en una década.
La COVID-19 deja al menos 214.000 muertos y más de tres millones de infectados en todo el mundo desde su aparición en China en diciembre pasado. Y amenaza con provocar la contracción económica global más grande en un siglo.
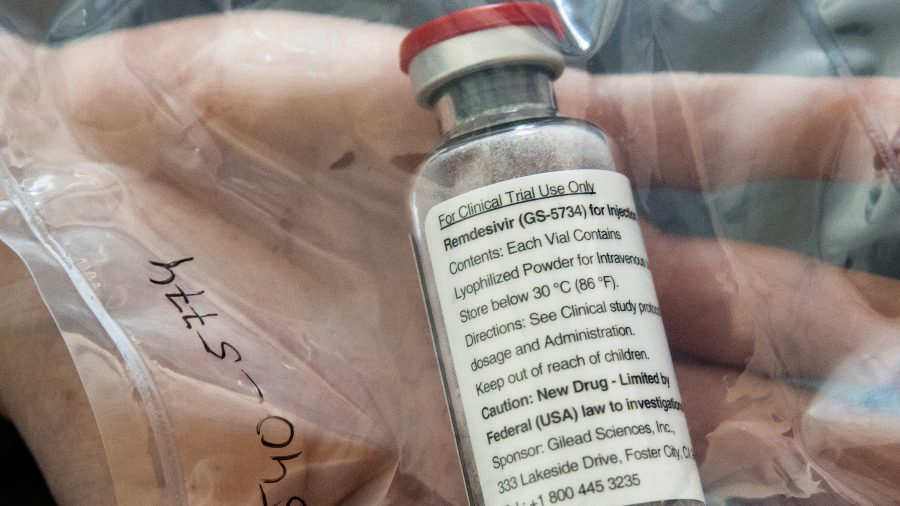
Pero una buena noticia disparó las bolsas mundiales: el laboratorio estadounidense Gilead reportó “resultados positivos” de un ensayo clínico con la droga remdesivir.
El principal epidemiólogo estadounidense y asesor del presidente Donald Trump, Anthony Fauci, que supervisó la investigación, dijo que el remdesivir “tiene un claro, significativo y positivo efecto en la disminución del tiempo de recuperación” de los enfermos de COVID-19.
Esto demostró que “un medicamento puede bloquear este virus”, afirmó en rueda de prensa en la Casa Blanca, comparando el hallazgo con los primeros retrovirales contra el VIH, el virus del sida, en los ańos 1980.
Fauci detalló que el tiempo medio de recuperación de los pacientes que tomaban la droga era de 11 días, comparado con los 15 días del grupo con placebos.
“Nos gustaría ver aprobaciones rápidas (por parte de la FDA), especialmente con las cosas que funcionan”, dijo el mandatario en una reunión en la Casa Blanca con empresarios.
La FDA seńaló este miércoles que ha estado llevando a cabo conversaciones “continuadas y sostenidas” con Gilead para hacer que Remdesivir esté disponible para los pacientes de COVID-19 “lo más rápido y adecuadamente posible”.
Un ensayo clínico más reducido realizado en Wuhan, donde se detectó por primera vez el nuevo coronavirus, contradijo estos hallazgos, según los resultados publicados en la revista médica británica The Lancet.
Pero Fauci desestimó este estudio, seńalando que no fue “adecuado”.
La Organización Mundial de la Salud (OMS), cuestionada por Trump por su gestión de la pandemia, anunció que su comité de emergencia se reunirá para evaluar la evolución de la situación el jueves, por primera vez desde que se declaró la emergencia internacional hace tres meses.
Pese a estas promesas de las autoridades, el laboratorio Gilead, con sede en Foster City (California), se mostró más cauta y enfatizó que Remdesivir no tiene licencia ni se ha aprobado en ninguna parte del mundo “y todavía no se ha demostrado que sea seguro o efectivo para el tratamiento de COVID-19”.

“Gilead compartirá en breve los datos adicionales sobre Remdesivir a partir de las pruebas de la compańía con COVID-19 grave”, ańadió el comunicado la empresa. “Este estudio proporcionará información acerca de si un tratamiento más breve, de cinco días de duración, puede tener una eficacia y seguridad similares al tratamiento de diez días en la prueba de NIAID y otras en curso”.
La firma indicó que espera tener para finales de mayo datos de un segundo estudio de evaluación de la eficacia de dosis de cinco y diez días en pacientes con COVID-19 moderada.
LAS PRUEBAS CON REMDESIVIR
Remdesivir no ha sido aprobado para el tratamiento de enfermedad alguna, pero ya se usó también de manera experimental con pacientes afectados por ébola.
El grupo tratado con remdesivir también mejoró levemente su expectativa de sobrevivir con una mortalidad de 8%, contra 11,6% en el grupo que recibió el placebo.
El estudio, que comenzó el 21 de febrero, involucró a 1.063 pacientes de 47 localidades en Estados Unidos y otros 21 lugares en Europa y Asia.
El primer paciente en recibir el tratamiento fue un estadounidense repatriado luego de permanecer en cuarentena a bordo del crucero Diamond Princess, y que recibió el medicamento en el centro médico de la Universidad de Nebraska.
La prueba fue realizada con un método llamado “el doble ciego” que implica que ni el paciente ni sus médicos tratantes sabían a qué grupo pertenecían, para eliminar el sesgos inconsciente.
Peter Horby, un epidemiólogo de la Universidad de Oxford que no participó en el estudio, seńaló que es necesario conocer los resultados completos. “Si se confirma esto podría ser un resultado fantástico y una gran noticia para la lucha contra el COVID-19”, dijo Horby.
Por su parte, Scott Gottliebb, excomisionado de la Administración de Drogas y Alimentos de Estados Unidos (FDA), escribió en Twitter que los datos bastan como para justificar que se considere una “autorización para uso de emergencia” del medicamento.
Una decisión como esa permitiría a los médicos a recetar el remdesivir fuera del contexto de los ensayos clínicos.
Beneficios genuinos pero modestos
El remdesivir, que había sido probado sin éxito contra el ébola, pertenece a una clase de medicamentos que actúan directamente sobre el virus, en lugar de controlar la respuesta autoinmune que genera, cuya inflamación puede ser letal.
La vía de acción consiste en replicar el ADN y ARN del virus para ser absorbido en su genoma y de esa manera impide que el patógeno se siga replicando.
En sus declaraciones a la prensa, Fauci dijo que el éxito de esta prueba podría allanar el camino para drogas más efectivas que apliquen un principio similar. Los hallazgos fueron celebrados por la comunidad científica, que igualmente advirtió que sus beneficios son relativamente modestos.
“Esta es la primera evidencia de que el remdesivir tiene beneficios genuinos, pero ciertamente no son espectaculares”, dijo Stephen Evans, experto en estadísticas médicas de la Facultad de Medicina y de Enfermedades Tropicales de Londres.
Por su parte Babak Javid, investigador principal de la Facultad de Medicina de Tsinghua, en Pekín, destacó que los datos son “prometedores”, aunque advirtió que el remdesivir “no es una solución mágica”.
En las últimas semanas hubo noticias disímiles y contradictorias sobre este antiviral intravenoso.
Un resumen de resultados publicado en el sitio web de la Organización Mundial de la Salud (OMS) la semana pasada mostró que no hubo resultados positivos en un ensayo más pequeńo realizado en China. La revista médica británica The Lancet publicó el miércoles el documento formal que describe esa prueba.
En el estudio de 237 pacientes en Wuhan, China, los médicos no encontraron efectos positivos tras la administración del medicamento en comparación con un grupo de control de adultos, a excepción de aquellos pacientes que requirieron ventiladores.
Pero la prueba china tuvo que detenerse tempranamente porque no podía reclutar a suficientes personas para alcanzar su objetivo inicial, y muchos expertos consideraron que por su reducido tamańo no permitía obtener conclusiones confiables.
En la búsqueda de una cura para la COVID-19 -que deja más de 220.000 muertos en el mundo desde su aparición en diciembre- los médicos han probado cloroquina y hidroxicloroquina, dorgas que se usn para combatir la malaria, bajo una modalidad llamada uso “compasivo”, que se utiliza cuando no hay tratamiento conocido.
También hay otras terapias en estudio incluyendo la recolección de anticuerpos de personas que hayan superado la enfermedad para inyectárselos a pacientes o recolectar anticuerpos de ratones genéticamente modificados que fueron infectados deliberadamente
Estados Unidos es el país más afectado por la pandemia, con casi 60.000 muertos y más de un millón de contagios. Le siguen Italia (27.000 muertos), Reino Unido (26.000) y Espańa (24.000).
En Europa, se investiga con preocupación la posible vinculación de la COVID-19 con una inflamación grave semejante a la enfermedad de Kawasaki, que afecta a nińos y adolescentes.